分子间的一种吸引力。
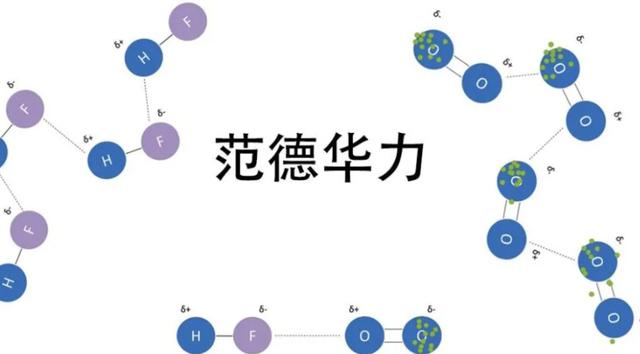
范德华力是存在于分子间的一种吸引力,它比化学键弱得多,一般来说,某物质的范德华力越大,则它的熔点、沸点就越高。
分子间作用力(Intermolecularforce)是指存在于分子与分子的作用力,包括作用在分子与其他类型的相邻颗粒(例如分子或离子)之间的吸引或排斥力。
分子间作用力相对于分子内作用力弱。
例如,涉及原子之间共享电子对的共价键比相邻分子之间存在的力强得多。
但两种作用力都是分子力学中的重要组成部分。
分子间作用力的研究始于宏观观察,这些观察说明了分子水平上力的存在和作用。
这些观察结果包括通过维里系数,蒸气压,粘度,表面张力和吸附数据反映的非理想气体热力学行为。
亚历克西斯·克拉劳特(AlexisClairaut)的著作《地物理论》中首次发现了微观力的性质。
为微观力研究做出贡献的其他科学家包括:拉普拉斯,高斯,麦克斯韦和玻尔兹曼等。
分子之间形成的氢键数目等于活性对数目。
提供氢的分子被称为供体分子,而含有参与氢键的孤对的分子被称为受体分子。
活性对的数目等于供体所具有的氢数目与受体所具有的孤对数目之间的公共数目。
尽管未在上图中示出,但是水分子具有两个活性对,因为氧原子可以与两个氢相互作用形成两个氢键。
与其他氢化物相比,分子间氢键是水沸点高(100°C)的原因。
范德华力存在于什么之中
范德华力之一
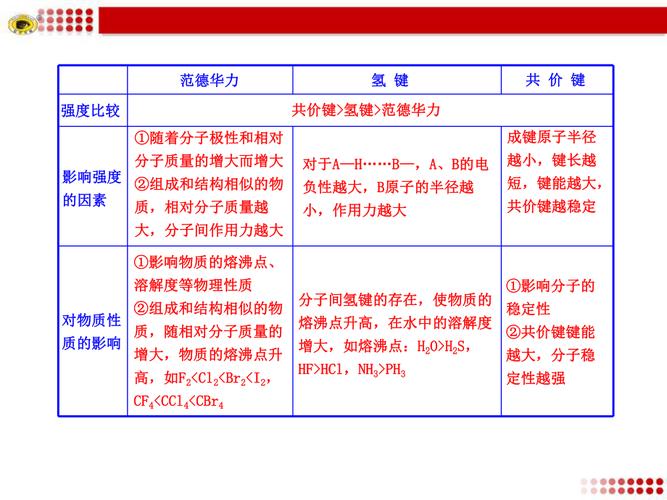
范德华力是存在于分子间的一种吸引力,它比化学键弱得多。一般来说,某物质的范德华力越大,则它的熔点、沸点就越高。对于组成和结构相似的物质,范德华力一般随着相对分子质量的增大而增强。
范德华力之二
范德华力也叫分子间力。
分子型物质能由气态转变为液态,由液态转变为固态,这说明分子间存在着相互作用力,这种作用力称为分子间力或范德华力。
分子间力有三种来源,即色散力、诱导力和取向力。
色散力是分子的瞬时偶极间的作用力,它的大小与分子的变形性等因素有关。
一般分子量愈大,分子内所含的电子数愈多,分子的变形性愈大,色散力亦愈大。
诱导力是分子的固有偶极与诱导偶极间的作用力,它的大小与分子的极性和变形性等有关。
取向力是分子的固有偶极间的作用力,它的大小与分子的极性和温度有关。
极性分子的偶极矩愈大,取向力愈大;温度愈高,取向力愈小。
在极性分子间有色散力,诱导力和取向力;在极性分子与非极性分子间有色散力和诱导力;在非极性分子间只有色散力。
实验证明,对大多数分子来说,色散力是主要的;只有偶极矩很大的分子(如水),取向力才是主要的;而诱导力通常是很小的。
范德华力之三
在物质的聚集态中,分子间存在着一种较弱的吸引力,作用能的大小一般只有每摩尔几千焦至几十千焦,比化学键的键能小1~2个数量级,亦称范德华引力或范氏力。
它由三部分作用力组成:①当极性分子相互接近时,它们的固有偶极将同极相斥而异极相吸,定向排列,产生分子间的作用力,叫做取向力。
偶极矩越大,取向力越大。
②当极性分子与非极性分子相互接近时,非极性分子在极性分子的固有偶极的作用下,发生极化,产生诱导偶极,然后诱导偶极与固有偶极相互吸引而产生分子间的作用力,叫做诱导力。
当然极性分子之间也存在诱导力。
③非极性分子之间,由于组成分子的正、负微粒不断运动,产生瞬间正、负电荷重心不重合,而出现瞬时偶极。
这种瞬时偶极之间的相互作用力,叫做色散力。
分子量越大,色散力越大。
当然在极性分子与非极性分子之间或极性分子之间也存在着色散力。
范德华引力是存在于分子间的一种不具有方向性和饱和性,作用范围在几百个皮米之间的力。
它对物质的沸点、熔点、气化热、熔化热、溶解度、表面张力、粘度等物理化学性质有决定性的影响。









还没有评论,来说两句吧...