共价键
原子间通过共用电子对所形成的相互作用,叫做共价键。
从下面几个方面掌握共价键:
(1)成键的微粒:一般为非金属原子(相同或不相同)。
(2)键的本质:原子间通过共用电子对(即电子云重叠)产生的强烈作用。
(3)键的形成条件:一般是非金属元素之间,且成键的原子最外层电子未达到饱和状态,则在两原子之间通过形成共用电子对成键。
(4)键能:分子中所含键的键能越大,分子越稳定。
(反应物总键能-生成物总键能)>0,反应吸热。
(反应物总键能)-生成物总键能<0,反应放热。
化学键的存在:
①构成稀有气体的单质分子,由于原子已构成稳定结构,在这些单原子分子中不存在化学键。
②在多原子单质分子中存在共价键,如CC2、I2、O3等。
③在多原子化合物分子中存在共价键,如HCl、H2O2、H2SO4等。
④在离子化合物中一定含有离子键,可能含有共价键。如K2O2、NaOH、NH4Cl等离子化合物中既有离子键又有共价键。
⑤在共价化合物中一定不存在离子键。
⑥离子化合物不一定都由金属元素和非金属元素组成。例如NH4Cl、NH4NO3等离子化合物中不含金属元素,只含非金属元素。
共价键强弱怎么判断方法
极性大小判断方法如下:
方法:
1、偶极距越大,分子的来自极性越大。
2、电负性相差越大,死补第共价键的极性也就越大。
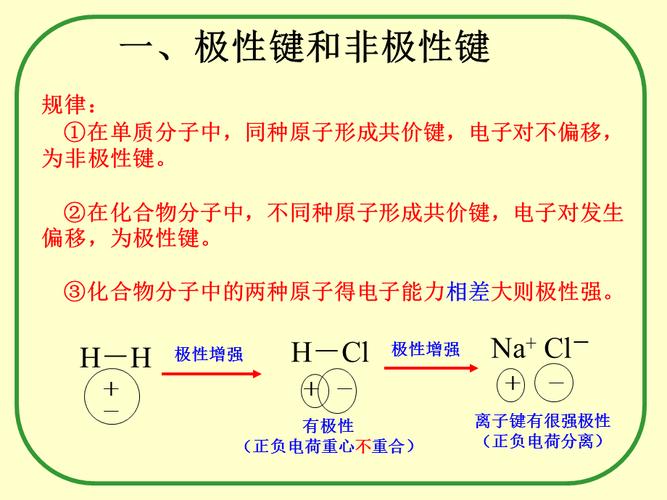
共价键的极性:
共价键的极性是因为成键的两个原子电负性不相同而产生的。
电负性高的原子会把共享电子对“拉”向它那一方,使得电荷不均匀分布。
这样形成了一组偶极,这样的键就是极性键。
电负性高的原子是负偶极,记作8-;电负性低的原子是正偶极,记作8+。
键的极性程度可以用两个原子电负性之差来衡量。
差值在0.4到1.9之间的是典型的极性共价键。
两个原子完全相同(当然电负性也完全相同)时,差值为0,这时原子间成非极性键。
相反地,如果差值超过了1.9,这两个原子之间就不会形成共价键,而是离子键。
分子极性判定标准及溶解性、熔沸点:
判定标准:
对于分子极性大小,目前尚无一个公认准确的量化标准,但比较常用的是根据物质的介电常数(尤其是液体和固体),对于一些简单的分子也可以根据其本身结构判断其是否有极性(如二氧化碳为直线型分子,为非极性化合物,但二氧化硫分子结构为V字型,故为极性分子)。
溶解性:
分子的极性对物质溶解性有很大影响。
极性分子易溶于极性溶剂,非极性分子易溶于非极性溶剂,也即“相似相溶”。
蔗糖、氨等极性分子和氯化钠等离子化合物易溶于水。
具有长碳链的有机物,如油脂、石油的成分多不溶于水,而溶于非极性的有机溶剂。
熔沸点:
在分子量相同的情况下,极性分子比非极性分子有更高的沸点。这是因为极性分子之间的取向力比非极性分子之间的色散力大。








还没有评论,来说两句吧...