糖皮质激素有强大的抗炎作用,能对抗各种原因如物理、化学、生理、免疫等所引起的炎症。
在炎症早期可减轻渗出、水肿、毛细血管扩张、白细胞浸润及吞噬反应,从而改善红、肿、热、痛等症状;在后期可抑制毛细血管和纤维母细胞的增生,延缓肉芽组织生成,防止糖连及瘢痕形成,减轻后遗症。
但必须注意,炎症反应是机体的一种防御功能,炎症后期的反应更是组织修复的重要过程。
因此,糖皮质激素在抑制炎症、减轻症状的同时,也降低机体的防御功能,可致感染扩散、阻碍创口愈合。
皮质激素抗炎作用的基本机制在于糖皮质激素(GCS)与靶细胞浆内的糖皮质激素受体(G-R)相结合后影响了参与炎症的一些基因转录而产生抗炎效应。
糖皮质激素的靶细胞广泛分布于肝、肺、脑、骨、胃肠平滑肌、骨骼肌、淋巴组织、成纤维细胞、胸腺等处。
各类细胞中受体的密度也各不相同。
G-R由约800个氨基酸构成。
其C端与GCS结合;其中央有两个锌指(zincfinger),各结合4个半胱氨酸;其N端的功能区τ1涉及与DNA结合后的转录性基因转移活化以及与其他转录因子的结合,人的G-R的结合功能区中还有τ2,它对受体进入核内有重要作用。
未活化的G-R与一大分子(约30kDa)蛋白质复合物相结合,该复合物含有两个热休克蛋白90(heatshockprotein90,Hsp90),其C端与受体相结合;该复合物可能还结合有其他蛋白,如抑制性蛋白等。
一旦GCS与G-R结合,Hsp90被解离,则被活化的GCS-G-R复合物迅速进入核内,进而与靶的基因的启动子(promoter)序列的糖皮质激素反应成分(glucocorticoidresponseelement,GRE)或负性糖皮质激素反应成分(negativeglucocorticoidresponeselement,nGRE)相结合,相应地引起转录增加或减少,继而通过mR-NA影响介质蛋白合成。
GCS可通过增加或减少基因转录而抑制炎症过程的某些环节,如对细胞因子、炎症介质及一氧化氮合成酶等的影响等。
细胞因子(cytokine)在慢性炎症起到重要作用。
它们能促进血管内皮细胞粘附白细胞,进而使其从血液渗出到炎性部位,并能使内皮细胞、嗜中性白细胞及区噬细胞活化,还能使血管通透性增加、刺激成纤维细胞增生以及刺激淋巴细胞增殖与分化。
GCS通过与G-R结合-nGRE的相互作用而抑制了一些与慢性炎症有关的细胞因子白介素1(IL-1)、肿瘤坏死因子α(TNFα)、巨噬细胞集落刺激因子(GM-CSF)、白介素3(IL-3)、白介素4(IL-4)、白介素5(IL-5)、白介素6(IL-6)及白介素8(IL-8)等的转录,而强烈地抑制细胞因子介导的炎症。
也有证据表明GCS可增加mRNA的断裂而使IL-1、IL-3及GM-CSF减少。
GCS也可通过抑制IL-2受体的合成,或通过将活化转录因子活化蛋白-1(activatorprotein-1,AP-1)等的活化调节逆转,或通过直接与AP-1相互作用,而对抗细胞因子的效应。
炎症介质,如白三烯(LT)、前列腺素(PG)等,前者有较强的白细胞趋化作用和增加血管通透性的作用,后者可引起红、肿、热、痛等炎症反应。
GCS可通过增加脂皮素(lipocortin-1)的合成及释放而抑制脂质介质白三烯(LT)、前列腺素(PG)及血小板活化因子(PAF)的生成,因为脂皮素(37kDa)可抑制脂质生成所必需的磷脂酶A2(PLA2)。
皮质激素还可以诱导血管紧张素转化酶(ACE)而降解缓激肽(可引起血管舒张和致痛),产生抗炎作用。
GCS可抑制巨噬细胞中一氧化氮合酶(NOsynthase,NOS)而发挥抗炎作用,因为各种细胞因子均可诱导NOS,使NO生成增多而增加炎性部位的血浆渗出,水肿形成及组织损伤,加重炎症症状。
(1)血液与造血系统皮质激素能刺激骨髓造血机能,使红细胞和血红蛋白含量增加,大剂量可使血小板增多并提高纤维蛋白原浓度,缩短凝血时间;促使中性白细胞数增多,但却降低其游走、吞噬、消化及糖酵解等功能,因而减弱对炎症区的浸润与吞噬活动。
对淋巴组织也有明显影响,在肾上腺皮质功能减退者,淋巴组织增生,淋巴细胞增多;而在肾上腺皮质功能亢进者,淋巴细胞减少,淋巴组织萎缩。
(2)中枢神经系统能提高中枢神经系统的兴奋性,出现欣快、激动、失眠等,偶可诱发精神失常。大剂量对儿童能致惊厥。
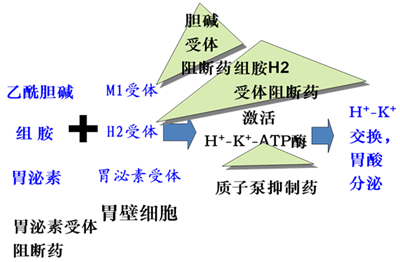
(3)消化系统糖皮质激素能使胃酸和胃蛋白酶分泌增多,提高食欲,促进消化,但大剂量应用可诱发或加重溃疡病。
口服、注射均可吸收。
口服可的松或氢化可的松后1~2小时血药浓度可达高峰。
一次给药作用持续8~12小时。
氢化可的松在血浆中(浓度小于25μg%时)约有90%以上与血浆蛋白结合,其中77%与皮质激素转运蛋白(transcortin,corticosteroidbindingglobulin,CBG)结合,CBG在血浆中含量少,虽亲和力大(3×10-7mol/L),但结合容量仍小;另有15%与白蛋白结合,其血浆含量高,结合量大。
CBG在肝中合成,雌激素可促进其合成,妊娠期间或雌激素治疗时,血中CBG浓度增高而游离的氢化可的松减少,但通过反馈调节,可使游离型者恢复正常水平。
肝、肾病时CBG合成减少,可使游离型增多。
吸收后,在肝分布较多。主要在肝中代谢,与葡萄糖醛酸或硫酸结合,与未结合部分一起由尿排出。
氢化可的松的血浆t1/2为80~144分钟,但在2~8小时后仍具有生物活性,剂量大或肝、肾功能不全者可使t1/2延长;甲状腺功能亢进时,肝灭活皮质激素加速,使t1/2缩短。
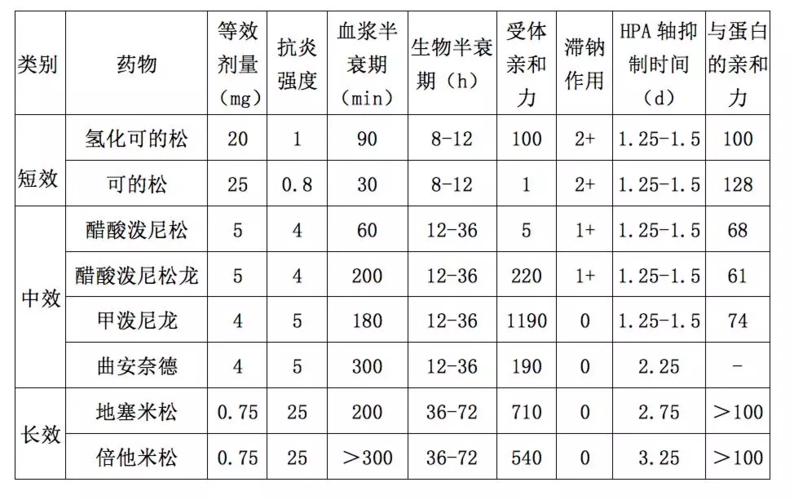
泼尼松龙因不易被灭活,t1/2可达200分钟。
可的松和泼尼松在肝内分别转化为氢化可的松和泼尼松龙而生效,故严重肝功能不全的病人只宜应用氢化可的松或泼尼松龙。与肝微粒体酶诱导剂如苯巴比妥、苯妥英钠等合用时需加大皮质激素的用量。
糖皮质激素与受体的结合方式
当多种激素共同参与某一生理活动的调节时,激素与激素之间往往存在着协同作用或拮抗作用,这对维持其功能活动的相对稳定起着重要作用。
例如,生长素、肾上腺素、糖皮质激素及胰高血糖素,虽然使用的环节不同,但均能提高血糖,在升糖效应上有协同作用;相反;胰岛素则以降低血糖,与上述激素的升糖效应有拮抗作用。
甲状旁腺激素与1,12-二羟维生素D3对血钙的调节是相辅相成的,而降钙素则有拮抗作用。
激素之间的协同作用与拮抗作用的机制比较复杂,可以发生在受体水平,也可以发生在受体后信息传递过程,或者是细胞内酶促反应的某一环节。
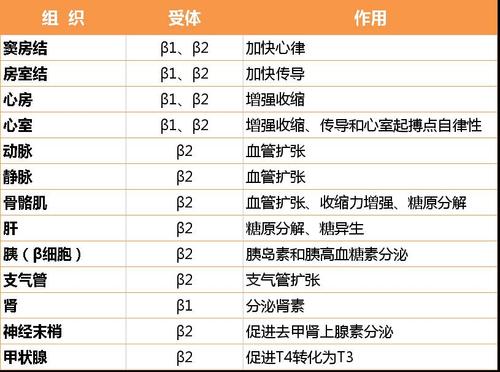
医学|教育网编辑整理例如,甲状腺激素可使许多组织(如心、脑等)β-肾上腺素能受体增加,提高对儿茶酚胺的敏感性,增强其效应。
孕酮与醛固醛在受体水平存在着拮抗作用,虽然孕酮与醛固酮受体的亲和性较小,但当孕酮浓度升高时,则可与醛固酮竞争同一受体,从而减弱醛固酮调节水盐代谢的作用。
前列环素(PGI2)可使血小板内cAMP增多,从而抑制血小板聚集;相反,血栓素A2(TXA2)却能使血小板内cAMP减少,促进血小板的聚集。
另外,有的激素本身并不能直接对某些器官、组织或细胞产生生理效应,然而在它存在的条件下,可使另一种激素的作用明显增强,即对另一种激素有调节起支持作用。
这种现象称为允许作用(permissiveaction)。
糖皮质激素的允许作用是最明显的,它对心肌和血管平滑肌并元收缩作用,但是,必须有糖皮质激素有存在,儿茶酚胺才能很好地发挥对心血管的调节作用。
关于允许作用的机制,至今尚未完全清楚。
过去认为,允许作用是由于糖皮质激素抑制儿茶酚-O-甲基移位酶,使儿茶酚胺降解速率减慢,导致儿茶酚胺作用增强。
现在通过对受体和受体水平的研究,也可以调节受体介导的细胞内住处传递过程,如影响腺苷酸环化酶的活性以及cAMP的生成等。










还没有评论,来说两句吧...